Warum diese Methode? Die Chemikalien sind vergleichsweise einfach zu bekommen, somit ist die Durchführung auch für uns Hobbywinzer realistisch.The Wittenham Hill Cider Portal hat geschrieben: 1. The Löwenthal Permanganate Titration
This was the standard method used at the Long Ashton Research Station from 1903 until the Cider Section's closure in the 1980's. The method relies on the oxidation of phenolics by potassium permanganate solution in the presence of indigo carmine as a 'redox indicator' to show the end point.
The following solutions are required. Both are sensitive to light and oxidation and should be prepared freshly on the day of use:
Potassium permanganate solution (N/40 or 0.005M). This may be made up from freshly diluted stock solution obtained from a laboratory supply house (generally as N/10 or 0.02M). Alternatively, it may be made up as required by accurately dissolving 0.79 g of analytical grade potassium permanganate in 1 litre of water to give the 0.005M solution.
Indigo carmine indicator. This is made up as a 0.1% working solution by dissolving ca 1 g of indigo carmine in 1 litre of water to which 50 ml of concentrated sulphuric acid has been added (take great care and wear eye protection when making up sulphuric acid solutions!! They can get very hot and bump violently. Always add the acid to the water and never the other way around!).
Procedure
Samples are analysed by adding 1 ml sample and 5 ml indigo carmine to the 500 ml flask and adding ca 200 ml water (tap water is fine for this). Titrate this against the permanganate solution until the royal blue fades to a light green. Then titrate dropwise until the lime green changes to yellow. Record this value as X ml.
A blank titration using 5 ml of indigo carmine alone in 200 ml water should also be carried out. The blank value should be ca 1 ml and should be recorded as Y ml.
With a little practice the endpoint is consistent to within 0.1 ml. It is advisable to work against a white tile or paper background in well lit conditions to see the endpoint more clearly. It is also helpful if the burette which contains the permanganate has a white background for easier reading of the scale, since this solution is intensely coloured.
Calculation of results
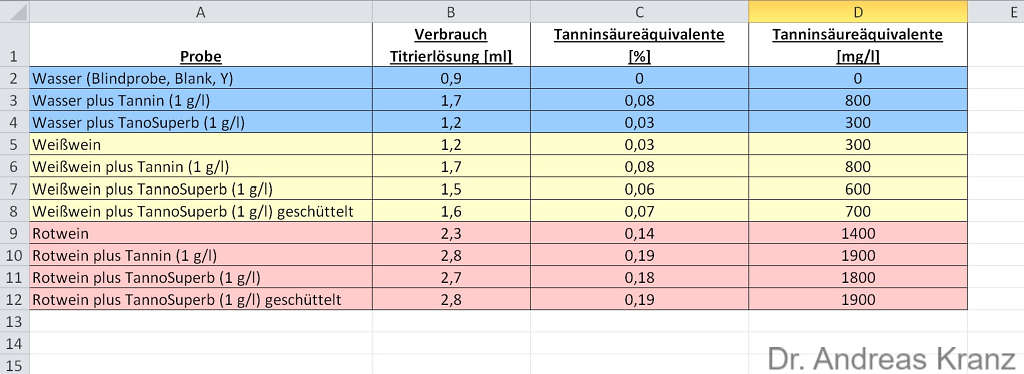
Total Tannin (%) = (X-Y)/10 expressed as 'tannic acid' equivalents.
To convert to ppm (parts per million or mg/l) multiply the tannin percentage figure by 10,000.
References
J. Löwenthal "Uber die Bestimmung des Gerbstoffs" Z. Anal. Chem (1877) 16 33- 48
Burroughs LF and and Whiting GC "Ann. Rept. Long Ashton Research Station for 1960" pp 140-143
Link zur Quelle: http://www.cider.org.uk/tanmeths.htm
Bevor man sich auf "reale" Proben stürzt muss man neue Methoden erst einmal etablieren und testen wo die Grenzen sind. Dazu plane ich einen Vorversuch, den ich hier dokumentieren will. Das Experimentelle Setup ist wie folgt:
- Zugabe von definierten Tanninmengen (1 g/l) zu Testflüssigkeiten
- Als Tannin teste ich parallel das Tannin einer Chemikalienbutze (siehe Dose) sowie Tanno Superb vom Belgier
- Als Testflüssigkeiten verwende ich Wasser, einen Rotwein und einen Weißwein

Da Tannine sich, je nach Herkunft, womöglich unwillig lösen will ich ihnen dazu genügend Zeit geben. Deshalb habe ich heute folgende Vorbereitungen getroffen:
- Ich habe jeweils 0,25 g Tannin in 0,25 L Flaschen vorgelegt. Eine dritte Flasche enthält kein Tannin.
- Mit Hilfe eines Standzylinders habe ich die Flüssigkeitsmenge abgemessen und in die Flaschen gegeben.
Noch ein paar Worte zur Theorie: Nach meinem Verständnis wird das Kaliumpermanganat als starkes Oxidationsmittel Tannin chemisch angreifen. Ist Tannin vollständig durch das Permanganat oxidiert, so greift dieses den Farbstoff Indigokarmin an, der hier als Indikator fungiert: Es kommt zu einem Farbumschlag von blau nach grün und schließlich nach gelb, was den Endpunkt anzeigt. Somit ist die verbrauchte Kaliumpermanganatlösung ein Maß für die in der Probe enthaltenen Tannine.
Zur Erinnerung: "Tannin" ist keine definierte Substanz, sondern ein Oberbegriff für eine Vielzahl verschiedener, aber chemisch verwandter Substanzen. Die genaue Tanninzusammensetzung ist von Pflanzenart zu Pflanzenart verschieden, verschiedenen Pflanzenteile können verschiedene Tannine enthalten. Speziell bei Früchten ist Menge und Art des Tannins auch vom Reifegrad abhängig. Es ist daher nicht zu erwarten, dass für die Permanganat-Neutralisation der beiden in diesem Versuch verwendeten Tannine exakt dieselbe Menge Titrierflüssigkeit benötigt wird. Insofern ist der Test nicht wirklich quantitatv, aber qualitativ: In Proben derselben Herkunft (zum Beispiel verschiedene Apfelsäfte, die eine ähnliche Tanninzusammensetzung haben sollten) kann ich mit der Titration aber durchaus bestimmen, in welchen mehr Tannin enthalten ist, selbst wenn der absolute Wert womöglich eine Hausnummer ist.
Laut der Quelle wird der Tanningehalt ausgerechnet und angegeben in "Tanninsäureäquivalenten"; Tanninsäure syn. Gallotannin gehört zu den Tanninen. Das ist so ähnlich wie bei den Säuren beim Wein: Auch wenn im Frucht- oder Honigweinwein womöglich gar keine Weinsäure enthalten ist, so dient sie doch als Referenz für die Angaben des Gesamtsäuregehalts.